Introdução - Objetivo
O HPV de alto risco causa câncer cervical, um desafio global para a saúde. O teste molecular de DNA permite a detecção precoce, permitindo o tratamento oportuno, melhorando o rastreamento, estratificando os riscos e otimizando o acompanhamento. Resultados confiáveis exigem desempenho laboratorial padronizado. Programas Externos de Avaliação da Qualidade (PEQA) acurácia (AC) e a harmonização no diagnóstico de HPV. Este estudo avalia o desempenho de laboratórios em um PQEA para detecção de HPV de alto risco, organizado por um provedor credenciado pela ABNT NBR ISO/IEC 17043:2011.
Métodos
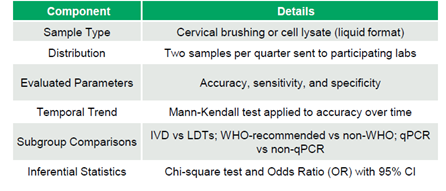
O PEQA consistiu em amostras líquidas de escovado cervical ou lisado celular. Os laboratórios participantes receberam duas amostras trimestralmente para avaliar a precisão, sensibilidade (SE) e especificidade (ES), que foram descritas detalhadamente. As tendências da AC ao longo do tempo foram analisadas usando o teste de Mann-Kendall. As comparações entre subgrupos incluíram kits de diagnóstico in vitro (IVD) versus testes desenvolvidos em laboratório (LDTs), kits recomendados pela OMS versus outros (não OMS) e métodos de qPCR versus não qPCR. Testes de qui-quadrado e razões de chances foram empregados para comparações estatísticas (Tabela 1).
Resultados
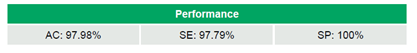
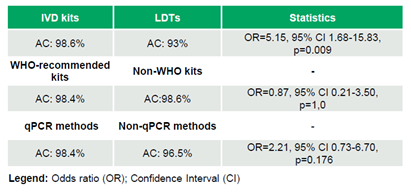
Entre 2020 e 2024, 69 laboratórios participaram de várias rodadas do programa, com uma mediana de 18 laboratórios/rodada (variação: 5–51), gerando um total de 692 conjuntos de dados (Tabela 2). Os laboratórios alcançaram 97,98% (678/692) de AC, 97,79% (620/634) de SE e 100% (58/58) de ES (Tabela 3). Não foram observadas tendências significativas na AC ao longo do tempo (τ = -0,046, p = 0,795). Os kits de IVD superaram os LDTs, alcançando 98,6% (612/621) de AC em comparação com 93,0% (66/71) (OR = 5,15, IC 95% 1,68–15,83, p = 0,009). Os kits recomendados pela OMS e os kits não recomendados pela OMS demonstraram taxas de AC comparáveis de 98,4% (185/188) e 98,6% (427/433), respectivamente (OR = 0,87, IC 95% 0,21–3,50, p = 1,0). Da mesma forma, os métodos de qPCR apresentaram desempenho semelhante aos métodos não-qPCR, com taxas de AC de 98,4% (541/550) versus 96,5% (136/141) (OR = 2,21, IC 95% 0,73–6,70, p = 0,176) (Tabela 4).
Conclusões
O PEQA para HPV de alto risco demonstrou desempenho diagnóstico robusto, com os kits de IVD superando significativamente os LDTs. Tanto os kits recomendados pela OMS quanto os não recomendados pela OMS, bem como os métodos de qPCR e não-qPCR, apresentaram AC comparável. Esses achados destacam a qualidade do diagnóstico de HPV nos laboratórios participantes e apoiam a preferência por testes de IVD para abordar a carga global de doenças relacionadas ao HPV.
Referências
WHO guideline for screening and treatment of cervical pre-cancer lesions for cervical cancer prevention, second edition: Use of mRNA tests for human papillomavirus (HPV)-World Health Organization, 2021.
Human papillomavirus (HPV) nucleic acid amplification tests (NAATs) to screen for cervical pre-cancer lesions and prevent cervical cancer: policy brief-World Health Organization, 2022.
Okada PA, Mitrat S, Rojanawiwat A. External quality assessment program for human papillomaviruses DNA testing in Thailand. Pract Lab Med. 2023 Dec26; 38: e00352. doi: 10.1016/j.plabm. 2023. e00352. PMID:38292923; PMCID: PMC10825476.