Introdução - Objetivo
Os laboratórios utilizam sistemas de monitoramento de desempenho, com indicadores de qualidade (IQ) desempenhando um papel fundamental. Erros pré-analíticos, responsáveis por até 70% dos erros laboratoriais, exigem monitoramento contínuo por meio de IQs. O Programa de Benchmarking de Indicadores Laboratoriais do Brasil, lançado em 2006, inclui 400 laboratórios de 17 países e 180 indicadores, 42 dos quais focados em IQs pré-analíticos. Este estudo tem como objetivo avaliar o desempenho dos laboratórios neste programa, com foco em sete IQs pré-analíticos harmonizados pelo Grupo de Trabalho sobre Erros Laboratoriais e Segurança do Paciente (WG-LEPS) da IFCC.
Métodos
O estudo avaliou sete indicadores pré-analíticos: Coleta de Amostra, Amostra Não Recebida por Erro de Transporte, Erro de Coleta (Amostra e Recipiente Incorretos), Amostras Coaguladas, Amostras Hemolizadas e Erro de Identificação do Paciente (solicitações identificadas incorretamente). Os valores medianos dos dados globais de 2018 e 2023 foram acessados, e o desempenho foi comparado usando métricas sigma (σ) para o 50º percentil para detectar diferenças.
Resultados
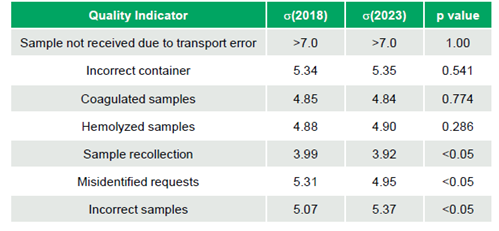
A análise não mostrou diferenças significativas entre 2018 e 2023 para quatro dos sete indicadores pré-analíticos (Amostra Não Recebida devido a Erro de Transporte σ >7,0 a >7,0, Recipiente Incorreto σ 5,34 a 5,35, Amostras Coaguladas σ 4,85 a 4,84, Amostras Hemolizadas σ 4,88 a 4,90; valores de p 1,00, 0,541, 0,774, 0,286, respectivamente). No entanto, diferenças estatisticamente significativas (todos os valores de p < 0,05) foram observadas para três indicadores: Coleta de Amostras (σ 3,99 a 3,92), Solicitações Identificadas Erroneamente (σ 5,31 a 4,95), ambos com desempenho reduzido, e Amostras Incorretas (σ 5,07 a 5,37), que apresentaram melhora (Tabela 1).
Conclusões
Embora algumas variações estatísticas tenham sido observadas, as métricas de desempenho sigma para a maioria dos indicadores permaneceram consistentes entre 2018 e 2023, destacando a estabilidade dos dados do programa de benchmarking. Os resultados sugerem que os laboratórios participantes podem não estar implementando ativamente ou podem não estar observando melhorias significativas nos processos pré-analíticos. Este estudo enfatiza a importância de esforços sustentados de melhoria, particularmente na coleta de amostras, para aprimorar o desempenho do laboratório.
Referências
Plebani M, Sciacovelli L, Aita A, Pelloso M, Chiozza ML. Performance criteria and quality indicators for the pre-analytical phase. Clin Chem Lab Med. 2015 May; 53(6): 943-8. doi:10.1515/cclm-2014-1124. Erratumin: Clin Chem Lab Med.2015Sep1;53(10): 1653. doi:10.1515/cclm-2015-7000. PMID: 25719322.
Sciacovelli L, Lippi G, Sumarac Z, Del Pino Castro IG, Ivanov A, De Guire V, Coskun C, Aita A, Padoan A, Plebani M; Working Group “Laboratory Errors and Patient Safety” of International Federation of Clinical Chemistry and Laboratory Medicine (IFCC). Pre-analytical quality indicators in laboratory medicine: Performance of laboratories participating in the IFCC working group «Laboratory Errors and Patient Safety» project. Clin Chim Acta. 2019Oct; 497:35-40. doi: 10.1016/j.cca.2019.07.007. Epub2019 Jul 8. PMID: 31295446.
Plebani M, Sciacovelli L, Aita A, Padoan A, Chiozza ML. Quality indicators to detect pre-analytical errors in laboratory testing. Clin Chim Acta. 2014May15;432: 44-8. doi: 10.1016/j.cca.2013.07.033. Epub 2013 Sep 5. PMID: 24012653.