Introdução - Objetivo
A sífilis, causada pelo Treponema pallidum, é uma das principais infecções sexualmente transmissíveis (IST) com impactos significativos na saúde, especialmente em ambientes com recursos limitados. Os testes POCT para sífilis são essenciais para o diagnóstico rápido e tratamento oportuno, oferecendo vantagens como facilidade de uso e aplicabilidade fora dos laboratórios tradicionais. Programas Externos de Avaliação da Qualidade (PEQA) são essenciais para garantir a precisão e a confiabilidade dos resultados, particularmente para infecções complexas. Este estudo avalia o desempenho diagnóstico de laboratórios participantes de um PEQA brasileiro (imunocromatografia) para sífilis, fornecido por um provedor de Ensaios de Proficiência (EP) credenciado pela ABNT NBR ISO/IEC 17043:2011.
Métodos
Foram analisados dados de 2010 a 2024, compreendendo quatro rodadas anuais do PEQA com quatro amostras de controle de qualidade liofilizadas e/ou líquidas por rodada. As métricas incluíram taxas de participação, adequação (%A), inadequação (%I), sensibilidade (SE) e especificidade (ES) para kits POCT comumente utilizados.
Resultados
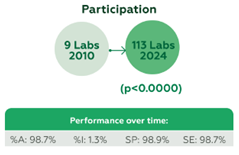
Ao longo de 14 anos, 348 participantes enviaram 12.555 conjuntos de dados. A participação cresceu de 9 laboratórios em 2010 para 113 em 2024 (p<0,0000). As métricas de desempenho permaneceram altas: %A 98,7%, %I 1,3%, ES 98,9% e SE 98,7% (Figura 1). Entre os 20 kits testados, 16 alcançaram %A >98%, com os kits mais utilizados apresentando resultados robustos:
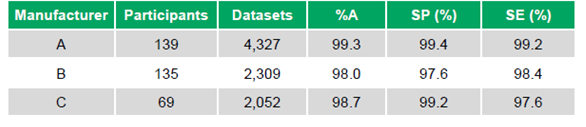
- Fabricante A: 139 participantes, 4.327 conjuntos de dados, %A 99,3%, ES 99,4%, SE 99,2%.
- Fabricante B: 135 participantes, 2.309 conjuntos de dados, %A 98,0%, ES 97,6%, SE 98,4%.
- Fabricante C: 69 participantes, 2.052 conjuntos de dados, %A 98,7%, ES 99,2%, SE 97,6% (Tabela 1).
Conjuntos de dados menores apresentaram correlação com desempenho inferior em alguns kits:
- Fabricante D: 7 participantes, 55 conjuntos de dados, %A 96,4%, ES 93,3%, SE 100%.
- Fabricante E: 5 participantes, 48 conjuntos de dados, %A 95,8%, ES 96,3%, SE 95,2%.
- Fabricante F: 3 participantes, 24 conjuntos de dados, %A 95,8%, ES 100%, SE 90%.
Conclusões
A adoção do POCT para sífilis no Brasil expandiu-se significativamente, como evidenciado pelo aumento da participação no PEQA e por fortes métricas de desempenho. Os PEQA garantem a confiabilidade dessas ferramentas diagnósticas, apoiando o aprimoramento do manejo de ISTs e na tomada de decisões clínicas.
Referências
Angel-Müller E, Grillo-Ardila CF, Amaya-Guio J, Torres-Montañez NA, Vasquez-Velez LF. Point of care rapid test for diagnosis of syphilis infection in men and non-pregnant women. Cochrane Database of Systematic Reviews 2018, Issue5. Art. No.: CD013036. DOI:10.1002/14651858.CD013036.
Taylor M, Alonso-González M, Gómez B, Korenromp E, Broutet N. World Health Organization global health sector strategy on sexually transmitted infections: an evidence to-action summary for Colombia [Estrategia global de la Organización Mundial de la Salud contra infecciones de transmisión sexual: de la evidencia a la acción. Resumen para Colombia.]. Revista Colombiana de Obstetricia y Ginecología 2017; 68(3):193-201.
Pan American Health Organization. Guidance on Syphilis Testing in Latin America and the Caribbean: Improving Uptake, Interpretation, and Quality of Testing in Di Herent Clinical Settings. Washington, DC. Pan American Health Organization 2015.
Peeling RW, Ye H. Diagnostic tools for preventing and managing maternal and congenital syphilis: an overview. Bulletin of the World Health Organization 2004; 82:439–46.